がん治療は、個々の状況に応じた個別化医療を行うことも普通になりつつあり、ほぼ全ての部位でステージ(がんの進行度を示す病期)が早期ほど5年、10年後の生存率が上昇しています。
がん治療は、個々の状況に応じた個別化医療を行うことも普通になりつつあり、ほぼ全ての部位でステージ(がんの進行度を示す病期)が早期ほど5年、10年後の生存率が上昇しています。
がん標準治療生存率
それでも、罹患率が増えている肺、膵臓、肝臓などの難治性の原発がんでは、ここ数年の生存率は変わっていません。
【目次】
がん標準治療を選択するとき
最悪のことを考えながらも、最善を尽くし、明るく生きたいものです
進行がん再発がんは標準治療だけでは治癒しない
治療の有用性と限界を知りましょう
各領域の専門性
がん治療は自分で納得して決めることも大切です
がんになる原因は、生活習慣などで遺伝子が後天的に変異することや、加齢により変異した遺伝子を排除できなくなることなど多くの要因に依存しますが、がんは早期に発見されるほど治療の成功率が高まります。現在は、患者さんのがんの種類、ステージ、遺伝子プロファイルに基づいて、個別に合った治療選択をすることが重要になっています。
がん標準治療は、治療効果や安全性が確認され現代、医学的に有効性が科学的根拠(エビデンス)により証明されている治療法です。機能を極力損なわないように根治的にがん組織を低侵襲(内視鏡・ロボット支援など)で摘出する外科治療(手術)。放射線科の画像診断部門で行われる各種画像診断、放射線治療部の行う緻密な照射ができる放射線治療。がん薬物療法専門医などが加わってがん細胞を抑制する薬物療法(化学療法、分子標的薬、免疫チェック阻害薬)など科学的根拠により有効性が証明されている治療法です。これらを組み合わせて総合的に治療する集学的治療をがん標準治療といいます。
第一選択は、手術や放射線などの局所治療
固形がんの治療は「局所治療」と「全身治療」に大きく分けられます。がんが発生した原発巣とその近傍の少数の転移であれば、 手術や放射線などの局所治療で“治癒”が期待できます。術前・術後に薬物療法を行うこともあります。
手術で根治が期待できないときや術後の再発・ 転移は全身病になります。そのため全身治療である薬物療法が必要になってきます。薬物療法では、細胞障害性抗がん薬や分子標的薬、免疫チェックポイント阻害薬があります。
科学的根拠の確立している標準治療でも限界はある
原発がんの部位、進行度に合わせて、標準治療から複数の治療法を組み合わせて行い進行がんでも、劇的に回復したケースも少なくありません。しかし、標準治療でも根治の限界はあります。がんのステージや病状が予後を大きく左右します。データだけでは、有用性や副作用が分からないなど、不確実なことはたくさんあるからです。手術が成功してもそれで完遂ではありません。それでも科学的根拠の確立している標準治療をやらないという選択は、効果的な治療法との出会い、長期間生存出来る可能性などを損なうことになります。
標準治療以上に自由診療(代替療法)の治療成績がよいということではありません
病理組織学的検査(生検)
病理学の分野においても発展にめざましいものがあり、免疫組織学、組織培養、画像処理による形態計測など新しい技術が導入されています。がんの手術では、病理医は、術中の患者さんの組織標本を受け取り、組織を-70℃で瞬時に凍結させて凍結標本を作製して術中迅速病理判定をします。術中に結果がでますので、外科医は病理の結果に基づいて切除範囲、リンパ節の郭清範囲を決めます。また、術後の病理検査でさらに詳しいことがわかり進行度を表す「ステージ」が決定されます。
画像検査だけでは確定診断はできませんので、担当科の医師が内視鏡などを使って組織を採取し、病理医が組織を顕微鏡で細胞の形やその並び方を観察してがんか否かの判断や悪性度(グレード)を決めます。内視鏡が使えない場合は超音波検査で、針を使って組織を採取します。病理診断は、内科や外科だけでなく、がんを扱う科にとって病理診断は確定診断の元になります。病理診断での確定診断は、その後の治療方針を決めることになります。
がんゲノム医療(DNAの全ての遺伝情報)
 ヒト細胞内の核には46本の染色体があります。染色体に含まれる遺伝子には2万3千個の遺伝子が存在しています。 ゲノムは、遺伝子をはじめとするすべての遺伝情報のことです。
ヒト細胞内の核には46本の染色体があります。染色体に含まれる遺伝子には2万3千個の遺伝子が存在しています。 ゲノムは、遺伝子をはじめとするすべての遺伝情報のことです。
遺伝子を幅広く調べる「がん遺伝子パネル検査」と少数の遺伝子を調べて診断する「がん遺伝子検査」があります。
中核拠点病院、拠点病院は自施設でに専門的な知識やスキルを有するがん薬物療法や病理学、分子診断学の専門医などがが参加する「エキスパートパネル」を開催して遺伝子解析による解析結果をもとに治療することができます。
医療連携病院は、連携する中核拠点病院または拠点病院のエキスパートパネルに依頼し遺伝子解析、分析します。結果は主治医に届きます。ただし、まだ個々の遺伝子異常に対応する治療効果が期待できる薬剤が揃っておらず、治療につながる患者さんは10-15%と少ない現状があります。がん遺伝子パネル検査は、遺伝子変異が検出されても適合する分子標的薬などがなく新たな治療につながらない場合もあります。
高性能の遺伝子解析装置「次世代シークエンサー」は多数の遺伝子異常を同時に測定する「がん遺伝子パネル検査」に用いられています。
※未だがんの発生の原因がわかっていない部分もありますが、治療を始める前に遺伝子などを検査して患者さんのがん遺伝子のタイプを調べます。その検査結果から有用性が高いと見込まれる薬を投与しますので、やってみないと有用性はわからないということは少なくなりました。
がん先進医療(精密医療)
※がんの組織や血液を使い、がん細胞の多くの遺伝子の変異を解析できる「がん遺伝子パネル検査」は、手術や抗がん剤などの標準的な治療を終えたがん患者さんに対して2019年に公的医療保険の適用になっています。
臓器横断的な治療とは、治療が特定の臓器に依存せず、がんの遺伝的または分子的特性に基づいて行われる治療法のことです。このアプローチでは、がんが発生した部位(例えば肺、肝臓、乳房など)ではなく、がん細胞の遺伝子変異や分子標的に基づいて治療が行われます。
最近の研究により、特定の遺伝子変異(例えば、※NTRK融合やMSI-H/dMMRなど)をターゲットにした薬物療法が開発され、臓器横断的な治療が可能となってきました。これにより、異なる臓器に発生するがんであっても、同じ遺伝子変異を持つがんは同じ治療法で対応できるようになっています。このアプローチは、患者さんに対してより個別化された治療を提供し、従来の臓器特異的な治療法では得られなかった効果を期待することができます。
※NTRK融合 NTRK遺伝子は、がん細胞の遺伝子異常の一つで、NTRK遺伝子が他の遺伝子と融合して異常な融合タンパク質を生成する現象です。この融合タンパク質ががんの成長と生存に重要な役割を果たしていることがわかっています。
※MSI-H/dMMR がんの遺伝的特性に関連する重要なバイオマーカーです。これらは特にがんの治療選択肢を決定する上で重要な役割を果たします。DNA修復機構の一つであるミスマッチ修復機構が機能不全になっている状態を指します。dMMRがあると、DNA複製時のエラーが修正されずに蓄積し、がんの発生リスクが高まります。dMMRは、MSI-Hと関連していることが多く、免疫チェックポイント阻害剤の効果を予測するバイオマーカーとして利用されています。
薬物療法(化学療法)
化学療法とは、抗がん剤を用いてがん細胞の増殖を抑制する治療のことです。抗がん剤は、複数の薬剤を組み合わせて使用する多剤併用療法は、異なる仕組みで作用する薬を用いることで、副作用も最小限に抑えてがん細胞に対しては増殖・増悪を抑えます。
代謝拮抗剤 、アルキル化剤、白金製剤などの種類があります。化学療法は、活発に増殖する細胞に対して治療効果はありますが、がん細胞だけでなく、特に活発に分裂している正常な細胞にも影響(副作用)が起こります。骨髄抑制(貧血、白血球、血小板減少)や肝臓、腎臓の機能障害など多くの副作用が認められます。それでも、がんの進行を遅らせることや、増殖、増悪を抑えがん巣の縮小効果を期待できます。 分子標的薬
がん細胞の変異に合わせたより効果的な分子標的薬を選んで治療するためのがんゲノム医療の「がん遺伝子検査」も普通になってきました。遺伝子変異を診断キットを用いて分子標的薬の使用を検討します。一人ひとりに合わせた治療を進める個別化治療も行われています。遺伝子パネル検査「ファンデーション・ワン」はがんに関連した324遺伝子を調べます。ヒトの体をつくる一つひとつの細胞は、2万個以上のの遺伝子によって構成されています。がん化する遺伝子変異は300以上発見されています。
免疫系が正常細胞とがん細胞を識別するのががん抗体(がん細胞にのみ過剰に発現するタンパク)があります。 異常なHER2の発現や遺伝子の増幅が、特に乳がんなどのがんで見られることがあり、 抗原に結合する分子標的薬トラスツズマブ(ヒト化モノクローナル抗体)エンハーツ、ハーセプチン抗悪性腫瘍剤などがあります。
EGFRは、細胞表面に存在するタンパク質の一種で、細胞の増殖、分化に関与する上皮成長因子受容体です。 異常な活性化や発現の変化ががんの発生と進行に関与することが知られています。 EGFRは4種類あり、遺伝子検査でEGFR遺伝子変異が確認された患者さんに投与することができます。標的治療薬には、EGFRチロシンキナーゼ阻害剤として、タルセバ、ゲフィチニブ、タグリッソやEGFRモノクローナル抗体、パニツムマブなどがあります。これ以外にも分子標的薬の適応になるBRAF遺伝子、RAS遺伝子などの異常もあります。抗上皮成長因子受容体(頭頸部扁平上皮癌)セツキシマブもあります。
古典的な抗がん剤に認められるような副作用は少ないのですが分子標的薬による副作用は薬の種類によってさまざまです。 がん細胞は免疫をくぐり抜ける仕組みがある
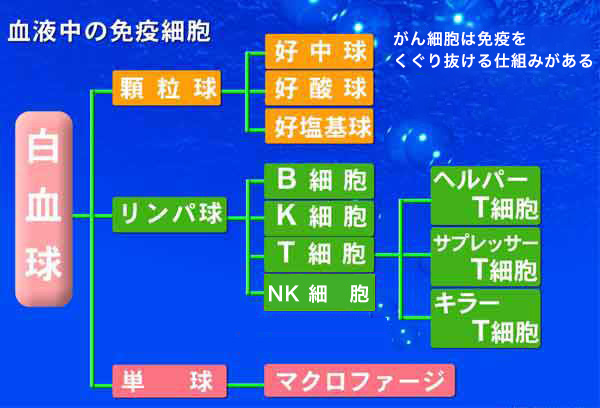 がん細胞は、免疫をくぐり抜ける仕組みがあり、がん抗原をT細胞受容体が認識しても T細胞はがん細胞を排除することができません。
がん細胞は、免疫をくぐり抜ける仕組みがあり、がん抗原をT細胞受容体が認識しても T細胞はがん細胞を排除することができません。
人間の白血球やリンパ球などの免疫システムががん細胞を異物としてみなさないからこそ、がん細胞は発生、増殖します。
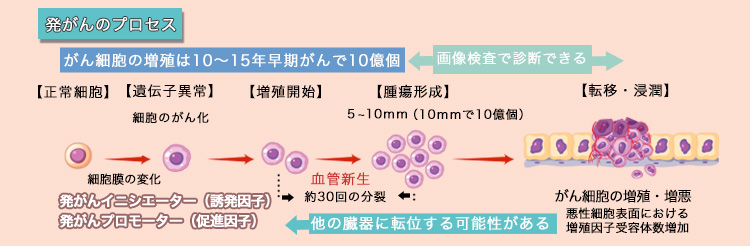
がん細胞が増殖する状態は、免疫細胞から排除されないために免疫抑制する環境を10〜15年くらいかけて一つの細胞にある2万数千個の一部の遺伝子が変異します。細胞が無秩序に増殖する、EGFR遺伝子、HER2遺伝子、RAS遺伝子など、100個以上のがん関連遺伝子がわかっています。
免疫細胞に排除されない状態にあると、細胞にある複数の遺伝子の突然変異によって正常細胞から異形成、がん細胞になり一つの細胞のがん化から増殖します。その過程で発がんイニシエーター(遺伝子の変化)・プロモーター(細胞膜の変化)も関わっていますが、最大の要因は加齢による細胞・遺伝子の老化です。人は年を取るだけで、遺伝子のダメージが増えます。もちろん生活習慣を改善することで、がんに罹患するリスクを減らすこともできます。
発がんのプロセス
増殖が速いものは悪性度が高く、遅いものは悪性度が低い
逆にがん細胞の性質が進行がんといわれる大きさになる以前に決まっているとすると、発見できる大きさになるまで転移しなかったがん組織は、それ以降も転移しない、と考えることもできます。発がんすると、がん細胞は細胞分裂を繰り返し細胞の数を増やしていきます。問題は、細胞分裂の速度です。速いものは悪性度が高く、遅いものは悪性度が低いと考えられています。
細胞分裂の速度が遅ければ、がん遺伝子変異の多段階発がんも遅くなり、また治るがんから治らないがんに移行するまでの期間が長くなると免疫システムの働きも活性化され、増殖・増悪・転移も抑えられるとも考えられます。
がん免疫療法 免疫チェックポイント分子
がん免疫チェックポイント分子は、免疫系の活性化や抑制を制御する役割を果たします。がん細胞が細胞膜に「T細胞の増殖」と細胞傷害を抑制する分子を発現していることがあります。目印となる分子にはCTLA-4とPD-1、PD-L1分子があり、これらの分子は、免疫系ががん細胞を排除する際に重要な役割を果たす免疫細胞の活性を調節します。それぞれが免疫チェックポイント阻害薬のターゲットとなっています。
多くのがん種では使用するタイミングや併用できる治療などは規定されているものの、採取したがん組織のたんぱく質濃度を調べた結果で遺伝子検査をせずに免疫チェックポイント薬を使えます。免疫系の活性化や、リンパ球の一つであるT細胞が活性化され、本来の免疫が働けるように促す作用があります。 がん細胞が免疫から逃れる仕組みを解除することで、がん細胞を異物と見なして排除することが可能になります。
免疫チェックポイント阻害薬が承認されてから10年ほど経ち、多くの医療機関で使われるようになったことで、標準治療のがん免疫療法は急速に進展しており、継続的な研究や臨床試験が行われています。将来的には、血中たんぱく質を検査機器で分析することで予測精度の向上も期待できます。新しい治療法や組み合わせ療法が開発され、がん治療のパラダイム(がん治療の捉え方)を変える可能性もあります。
薬物療法(抗がん剤)
最悪のことを考えながらも、最善を尽くし、明るく生きたいものです
手術でがん巣を摘出すれば、かなりの治癒率が期待できるものの進行した段階で発見され、転移が見られるような場合には根治的手術による治療は限界があります。生活の質(QOL)の改善を目的とした姑息的治療が行われます。
「姑息」という言葉は「一時的な」「対症療法」という意味です。 手術で治癒が望めない段階になって診断された場合や再発したときなどには、抗がん剤治療や放射線治療が行われます。それでも一時的にがん巣を縮小することができても多くの場合、決定的な治療法とはなりません。
問題は副作用です。白血球の減少などの骨髄抑制、腎機能の低下など、さまざまな副作用をともないます。また当初、抗がん剤でがん巣を小さくできても、やがてがん細胞のほうに耐性ができ効かなくなります。再び腫瘤が増殖、増悪して遠隔転移も認められてくると、それまでの抗がん剤では抑えることができなくなりますから、違う抗がん剤を使用することになります。
薬剤耐性が出るのは、がん細胞の多様性があるからです。 例えば1次治療(ファストライン)の抗がん剤での効果が乏しくなったときは2次治療(セカンドライン)に移行します。 ゲノム検査で有効性のある薬剤が適応になるならよいのですが有用性のある薬剤の選択は少なくなります。その次は、3次治療(サードライン)ですがそこまでの薬剤投与は、体力的にも副作用で難しくなります。
これまでのがん治療の歴史から、抗がん剤を無理に受け続けることの是非が問われるようになり、最近それを裏付ける質の高い臨床研究が報告されるようになってきました。しかし、がんの増殖速度が著しく速い場合、現状として直接的にがんの勢いを抑える効果が期待できる治療として、抗がん剤を上回る治療の存在は示されていません。
再発・転移がわかった場合、やはり抗がん剤投与します。がん治療の歴史はそうでした。標準治療では、がん細胞が増悪・増殖しない安定した状態の「無増悪生存期間」を延ばすことが目的になります。がんの種類、性質、体質、体力を鑑みて、作用機序の異なる薬の選択や組み合わせを決めたりして治療を進めます。
がん組織では、多様ながん細胞がありその中のがん細胞が必ず変異して薬剤耐性を獲得します。何度も繰り返し投与しているうち、ついには、あらゆる抗がん剤が有効性を示せなくなります。身体の免疫抵抗が壊滅状態になってきます。やがてほとんど治療効果がなくなったとき、患者さんがなんとか治療を続けたいと願っても「これ以上、治療する手段がありません」といわれることになります。
長期にわたってコントロールする
最近の治療では、従来からの古典的な抗がん剤や分子標的薬、免疫チェックポイント阻害薬などで上手く長期にわたってコントロールできれば、良い体調を保ったままがんになる以前の生活を続けることができるだけでなく、がんで亡くなるのではなく寿命を全うすることもできるからです。
抗がん剤の利益と副作用の不利益
抗がん剤治療を専門的に行うメディカルオンコロジスト(がん薬物療法専門医)だけではなく、がんにかかわる診断・治療などを行う医療従事者は抗がん剤治療を続け、進行がんの場合でも、あたかも標準治療では、ぎりぎりまで抗がん剤治療をほとんどのケースで行います。
抗がん剤の利益と副作用の不利益を患者さんも詳しく話をしてほしいとこです。効果よりも副作用が明らかに上回るようになった場合、当然ですが抗がん剤治療は受け続けるべきではないでしょう。 緩和ケアは、治療不能な病気や痛みと向き合う際に、生活の質を向上させる
もちろん全ての抗がん剤治療を否定しているわけではありません。 抗がん剤治療をはじめて腫瘍マーカーも下がり、パフォーマンスステータス(患者さんの日常生活の制限の指標)も向上した患者さんもたくさんいました。それでもギリギリまで標準治療を続けるのではなく、早期の緩和ケアの選択も大切です。その方がどれだけ患者さんに有意義な時間が取れるか。是非理解してほしいところです。在宅療養支援診療所・在宅療養支援病院なども余裕を持って利用するのも一考です。
丁寧な説明をしてほしい
半数近くの方は、病院で死を迎えています。だからこそ医者の言葉は重く、患者さんや家族は医者の一言に一喜一憂します。
がんの告知や治療方針あるいは余命宣告が普通にはなりましたが、特に若い医者に多いのが患者さんの病気と真っ向から向き合う気持ちがないのか、患者さんの気持ちを無視している場合があります。当然本人は悪意はなくても、患者さんの心は傷つきます。そんな相談も多いです。典型的なパソコンの画面を見て話す医者ですね。人間の心の微妙なことがわからないのです。
期待していたのに、自分の期待感より満足度が低いと、この気持ちが自分の中でストレス、不安感を生んでしまいます。 患者さんも「標準治療を受けていれば安心」と、思っている人は多いのですが主治医も「これが標準治療です」と、マニュアルに書かれた治療を提供します。
治療におけるやってほしいこと、やってほしくないことなど自分の考えを伝え、事前に医療者側と大筋で合意しておいた方が良いと思います。遠慮なく話すことでお互いの考えを明確化して、ふわっとした期待感による無用なすれ違いを起こさないことも大切なことです。
進行がん、再発がんは標準治療だけでは治癒しない
複数の遺伝子にダメージが徐々に蓄積していくと遺伝子変異する人間の体は約60兆個の細胞でできており、全ての細胞には細胞周期があり、細胞は絶えず一定の法則に従って分裂増殖しています。そのため正常細胞はアポトーシス(古くなった細胞の自然死)して新しい細胞におきかわります。ところが、細胞のがん化は何らかの原因によって細胞の複製に必要な複数の遺伝子にダメージが徐々に蓄積していくと遺伝子変異します。
タンパク質、炎症性サイトカインも関与している要因もあり、細胞にとって、異常に増殖する可能性のある環境が作られてしまうこともあります。全て証明されているわけではありませんが発がん要因の影響度は、発がん物質(イニシエイターン)と、がん促進物質(プロモーター)に分類されます。
がん抑制遺伝子、免疫の力で体外に排除される
それ自体は健康な人でも日常起こっていると考えられています。そして変異した細胞の多くはがん抑制遺伝子、免疫の力で体外に排除されますが、なかには異常増殖を引き起こすものもあります。 それが何年もの時間をかけて異常な増殖を繰り返して、がん細胞は塊(組織)になって「腫瘍」を形成します。全身のあらゆる臓器、部位に発生します。がん化した細胞の組織型は多数あり、腺癌、扁平上皮癌、小細胞癌などと組織型も分類されています。未分化がんは、細胞としては未熟な状態で悪性度は高いです。
転移するメカニズムはとても複雑で難しい
「原発巣」は、手術や集学的治療の進歩で、かなり治療可能になりました。原発巣が原因で死ぬことは少なくなりました。 転移したがんの増殖を抑えることができる方法が見つかれば、がんによる死亡率は激減します。
しかし、転移するメカニズムはとても複雑で難しくその発症メカニズムは完全に分かっていません。がん細胞に遺伝子変異が加わることによって、遠隔転移する能力を獲得するのか、それとももともとのがん細胞に最初から転移する能力があったのか現在の医学では、仮説はありますが、本当のことは分かりません。
証明するのは困難ですので、転移が認められない場合(画像検査でも5~10mm以下の転移巣を発見することはできませんので、正しくいうと転移巣があっても画像上発見ができない)、多くのケースで手術が選択され原発巣の摘出がおこなわれます。ですが原発巣を摘出しても数年後、再発することも珍しくはありません。術後補助療法としての抗がん剤を投与しますが、それでも再発するときは再発します。放射線療法も予防的効果は未知数です。
再発、遠隔転移してしまった場合は深刻治療は固形がんの場合は手術が中心となり完治された方は多数います。ところが手術後、再発、遠隔転移してしまった場合は深刻になります。患者さんの命を助けようと懸命に努力している医師、そして闘病生活を送っている患者さんに対しては申し訳ないのですが、多くの人が感じているように極端な言い方をすれば、これらの集学的治療は早期がん・転移しないがん、治るがん以外では限界に来ています。
確かに、腫瘍マーカーやCT、エコー、MRI、PETなどさまざまな検査方法が登場して精度が上がったため、腫瘍の把握が可能になりました。
しかし、進行がんイコール末期がんではありませんが、例外はあるかもしれないけど、標準治療だけでは治癒しないという事実を知ってほしいです。
悪性度の高い進行してしまった難治性のがんにおいては、どうしようもない状況は10年前、20年前、30年前と比較してもほとんど変わっていません。
手術後に再発をくりかえしたり、或いは手術が出来ないほど原発巣が隣接臓器まで浸潤していたり、遠隔転移している場合は化学療法オンコロジスト(腫瘍専門内科医)が治療にあたる事が望ましいと思いますが、まだ日本では腫瘍専門内科医の数が少ないのが現状です。
がん細胞転移阻害剤
薬物療法でがん細胞の増殖を抑えたりする治療は全身療法になります。正常細胞にダメージを与えますがそれ以上にがん細胞にダメージを与えます。 薬物療法では、病勢の増悪や重い副作用がない限り、現状の治療を継続するのが基本です。転移するがん細胞をターゲットにした「転移阻害剤」は、開発されていません。 分子標的薬にも副作用がある
また最近では「分子標的薬」が使用されることも多くなってきました。しかし分子標的薬にも副作用の問題があります。しかも従来の化学療法の抗がん剤の副作用はある程度はパターンが分かっていたのですが、分子標的薬はより対応が難しい面があります。全てのがんではありませんが、がんが進行した場合、これらの治療方法は延命することを期待するしかない現状は長年変わっていません。
「免疫チェックポイント阻害薬」も有効率は約10%と期待値を下回っています。遺伝子変異に合う薬剤投与ができた患者さんは遺伝子検査を受けた方の全体の20%以下です。
Tリンパ球に働きかける免疫療法
国内の医療機関10カ所で免疫治療薬(がん細胞に直接作用するのではなく、がん細胞を抑制するTリンパ球に働きかける免疫療法の薬剤)の治験を実施した結果を2020年5月、 米国臨床腫瘍学会特別臨床科学シンポジウムで発表されました。
原発巣特定できない原発不明がんは、非常に治療が難しいのですが、 商品名:オプジーボの投与により効果があった中央値は12・4カ月で、原発不明がんで最も一般的な治療法の約2倍の有用性があったとの報告がありました。一時的にがんが巣が小さくなったかどうかよりも、がんの進行を抑えられた期間が評価される時代です。
制約もありますが、遺伝子パネル検査で、たくさんの遺伝子変異を調べられるようになったので、将来有効な化学療法療にまでつなげることができる可能性もあります。
少数転移(オリゴメタスタシス)
大腸がん以外のがんではガイドライン等で、明確に記されていませんが、がん細胞が広範囲に転移する能力を獲得しておらず、少数個のがん巣の転移のみ存在する状態の患者さんが少数ですが、いるとも考えられています。 多くの種類のがんで認められ、転移しない限局がん、と多発転移する状態の中間的状態の少数転移(オリゴメタスタシス)と呼ばれています。しかし転移病巣に対する切除に対して、その確定診断法は定かになっていません。
新薬の臨床試験も毎年行われています
最先端治療、新しい薬物療法も、最善の治療のことではありません。ランダム化比較試験(多くの手間がかかりますが、治療効果の程度を数字で表すことができます)が行われて初めて有効性が証明されます。「ランダム」とは日本語で「無作為」と訳します。人為的な操作が入り込まないということを意味しています。一番信頼のおける臨床試験です。副作用や安全性も考慮して行われています。いくつかの臨床試験も毎年行われていますがそれでも承認される国産の抗がん剤は少ないです。
日本の行政は方向転換が苦手で、過ちを正すのにあまりにも時間をかけすぎるとこがあります。がんの罹患率、亡くなる方も増えています。これを高齢化にともなう現象として諦めて、受け入れるべきなのでしょうか。世界に共通する現象ならまだしも、海外に目を向ければ、アメリカなどは、がん(悪性新生物)死者数が減少に転じています。標準治療で、がん死者数の増加を食い止められないのであれば、抜本的な見直しを図るべきです。
通常のがん治療(標準治療)の有用性と限界を知りましょう
原発がんの早期発見は有用性はあるかもしれませんが再発の早期発見はあまり有用性はない
基本的には完全に治すことはできなくなるのですが、再発転移の告知は難しいのはわかりますが、時間をかけて話すことも少なくはっきり伝えずに「がんが再発しました。でも引き続き治療をしていきましょう」とだけ伝える場合が多いのですが、 それで患者さんは「治療すれば治るんだ」と期待してしまいます。
再発・転移が見つかった時点で、がんは全身病になります。どんな治療をしても、完全には治すことは難しくなります。
再発・転移がんを完治できないまでも、早く発見して抗がん剤、放射線で叩いた方が、 延命できるのではないか、そう考えになるかもしれません。ところが、いくら早く転移がわかって早期に治療しても延命効果は、あまり変わりません。自覚症状もないのに抗がん剤治療になり副作用は自覚症状が有る無いに関わらず必ずあります。
再発がんは、どこにできたがんにしろ治療は難しくなります。再発・転移を予防する薬剤、治療法はありません。CTやMRIは組織の形態を観察するための検査法で、PTE検査は生体の機能を観察することに特化した検査法ですががん巣の拡りがある程度わかるだけです。 わかるだけで治るわけではありません。
現在、細胞のがん化については未だに解明されていません。生物学(自然界で生きているあらゆる「生物」を研究する学問)・医学(臨床・基礎研究)では、再発・転移した場合標準治療であろうと、革新的な治療であっても持続的な奏効をもたらすがんの治療法は存在しません。
それでも現時点で一番いい治療は保険適用となっている標準治療です。作用機序の異なる薬剤でがんの種類、性質、体質、体力(治癒力)を鑑みて、薬の選択や組み合わせを決めたりして治療を進めます。できるだけ長期間にわたってがんの病変をコントロール(増悪・増殖を抑える)して、無増悪期間を保ったままがんになる以前の生活を続けることが目標になります。長期にわたってコントロールできれば、がんで亡くなるのではなく寿命を全うすることもできるからです。 がん細胞の不均一性
遺伝子を含む染色体、解析により、同じ人にできるがんでも進行する過程、転移の部位が変わるうちに原発とは別の遺伝子が発現することがわかってきました。薬物治療を翻弄するジレンマも出てきました。「遺伝子変異」は今や「多様性」と考えるべきです。 同じ臓器のがんであっても異なる複数の細胞によって構成されています。 これを「がん細胞の不均一性」といいます。
「がん細胞の不均一性」を考慮しなくては、今の画一的な標準治療では十分な効果は期待できないと思います。遺伝子を含む染色体、解析により、同じ人にできるがんでも進行する過程あるいは、転移の部位が変わるうちに原発とは別の遺伝子が発現することがわかってきました。
これが抗がん剤に対してがん細胞が耐性を獲得する理由です。 最初は有用性もあり利益(ベネフィット)もありましたが後に、 必ず薬剤から生き延びるがん細胞がいますので増殖してきます。がん細胞の多様性があるからです。
一般的に、術後、再発を抑えるためと称して抗がん剤による療法が行われることが多いのですが、再発する、しないは個人差あるいは、がん腫の違いがあります。 術後の抗がん剤を行うか否か、行う場合にはどれくらいの期間抗がん剤治療を行うことが、その方の利益(ベネフィット)なのかまだわかっていません。
再発してしまう可能性が高い場合もありますが、再発の心配がほとんどないと考えられる場合もあります。それでも再発の抑制になるのかわかりませんが、抗がん剤の投与をする場合は多いです。遺伝子(ゲノム)検査で過剰な抗がん剤投与を控えるための研究も進んでいます。
生体にダメージを与えないで治療効果を出す本当の意味で個別化された、がん治療が求められています。 遺伝子を調べて薬物療法に役立てる検査「遺伝子パネル検査」も保険適用になりましたが、分子標的薬、免疫チェックポイント阻害剤、抗体薬物複合体などの有効的な薬剤を投与できる割合は15%くらいです。
よく知られている遺伝子に「BRCA」があります。DNA(デオキシリボ核酸)に生じた変異を修復するBRCAタンパク質は細胞のがん化を抑える遺伝子です。BRCAタンパク質の異常があると遺伝性乳がん・卵巣がんだけではなく食道がん、胃がん、胆道がんを発症しやすくなることはが改めてゲノム解析で確認されました。それでも、なぜ特定の細胞ががん化するのかヒトゲノムの完全な配列を解析することができた現在も根本的なことはわかっていません。
固形がんの場合、外科手術はがん治療における第一選択肢です。手術でがん巣を取りこぼしなく摘出します。またIMRT(強度変調放射線治療)は腫瘍だけに高い照射線量を照射することができます。手術や放射線などの局所治療が有効です。全身治療として、抗がん剤もありますが今後はケミカルサージェリー(光、超音波、熱中性子線を患部にピンポイントで照射する手技)、ドラッグデリバリーシステム(中性子捕捉治療など)も次世代の治療法の選択になるかもしれません。
光免疫療法(頭頸部がんや皮膚がんなどの表在性腫瘍に対して研究が進められています)
新しいがん治療法の一つで、薬剤アキャルックス®2時間以上かけて点滴で投与し、20~28時間後にレーザ 光照射を行う治療です。この治療法は、特定のがん細胞を標的として破壊し、同時に免疫系の反応を引き起こすことで、がんの制御を目指します。
がん細胞の表面には増殖のシグナルを送るタンパク質EGFRが多く存在しています。アキャルックス®(効果的な治療のためには、がん細胞の特異的な抗原を認識する適切な抗体を選択する必要があります)は、このEGFRに結合します。結合したがん細胞に全身麻酔を行い、手術室で体の外から当てる方法と、皮下組織(体の中)にあるがん巣に針を刺し、レーザ光を当てることによりアキャルックス®含まれる色素が反応します。
反応したがん細胞の細胞膜に特定の波長の光を照射します。この光は、光感受性物質を活性化させ、がん細胞を選択的に破壊します。治療は3日で完了しますが1ヶ月程度は直射日光に当たらないようにする注意も必要です。
光によるがん細胞の破壊は、破壊されたがん細胞から、がんに対する免疫反応を引き起こします。免疫系の抗原が活性します。これにより、治療後も残存がん細胞の排除が期待されます。
光免疫治療は、特に頭頸部がんや皮膚がんなどの表在性腫瘍に対して研究が進められています。他のがん種や治療法との併用によるさらなる研究が期待されています。太い血管を巻き込んでいる場合使用できないことや、副作用もありますが、この治療法は、がん治療の新しい選択肢として注目されており、特に従来の治療法に抵抗性を示すがんに対して、効果的な治療法となる可能性もあります。
各領域の専門性
今の診療は大学病院をはじめがん専門病院など各専門分野に分かれています。学会もかなり専門分野に分かれています。 もちろん病気は慢性疾患を含めて多数あります。
がんの病気だけでも日本がん学会を初め各領域の専門性があり、例えば「胃がん」を扱う医学学会でも、外科学会、消化器外科学会、胃がん学会、がん治療学会など多くの学会があり、毎年総会が開かれ多くの演題が発表されます。
また各領域の「認定医」「専門医」「指導医」の制度もあります。この制度は高度な知識や技術、経験など資格審査もあり一般的に考えて肩書きのある医師の専門性に期待できます。「認定医」「専門医」にならなければ、違う領域の診療、治療出来ないと言うことはないのですが、それだけ専門性が問われる医療システムになってきたということです。
当然ですが誰でもその領域の症例数が多く治癒率も高い信頼のおける医師に総合的に治療を受けたいと思うでしょう。
がん治療は自分で納得して決めることも大切です
標準治療ベストな治療法を選択確かにがん巣が一つの臓器に留まっている限局では部分病との解釈もできるかもしれません。 当然ステージも低いので治癒できる可能性は高く治療法の第一選択も手術だけではありません。
治療面は、相当前から手術や薬剤あるいは、放射線など集学的治療に頼るしかなく、根治的な治療ができているわけではありませんでした。 現在は、 手術でも手術支援ロボット、鏡視下手術術も普及してきました。またがん細胞だけにピンポイントで放射線を当てることも可能になり、薬物治療と併用することで高い治療効果を上げています。
「分子標的治療薬」「免疫チェックポイント阻害薬」などは様々ながんの生存率を引き上げる可能性があります。がんと診断されたとき大切なことは全て病院任せ、医者任せにしないことです。積極的に治療法を医療者側から聞きましょう。そして治療法を納得して決めることも大切です。
原発巣から他の部位に転移した場合、がんは全身病になります。 治療手段も限られてきますので、患者さんの治療は同一には行えません。がん診療拠点病院では各種がんの生存率を公開しています。医療の透明性確保、患者さんの自己決定権の尊重があるからです。その上で治療法の決定に至る過程は様々ですがオーダメード治療が重要になってきます。
インフォームドコンセント「正しい情報を得た(伝えられた)上での合意」で納得のいく治療を選択しましょう。
がん細胞の遺伝子構造は一人一人異なり、一つとして同じがんの遺伝子はありません。
だから治療法も人それぞれ違う。標準治療でも「これが絶対」という治療法はないのです。
がんの転移には、がん幹細胞が関係していますが治療ではあまり考慮されません。
主治医とは納得できるまで話し合い信頼関係を築きましょう。主治医の個人的な意見に留まらず、考えられる治療法についての説明を受けましょう。そして、がんについての知識を集め納得する治療の選択をしましょう。
受けられる治療法の効果と限界、危険性や副作用を知りましょう。
できれば生涯付き合えるような信頼できる医師を選ぶことです。
説明と同意(インフォームド・コンセント)が大切なことだとわかりますが、その結果どうなったか。極端な例は医者は説明だけして、患者さんに決めさせるスタイルになってきました。
いままでは医者のいうままに副作用にも耐えて抗がん剤治療してきたのに、がんが進行して治療法が行き詰まってくると、あなたの選択肢はこれだけですから、あとは自分で決めてくださいと患者さんを困惑させるやり方です。
本来なら、治療の選択肢について、それぞれのメリットとデメリットを時間をかけて納得するまで説明し、そのうえでどうするかを一緒に考えていくのが医療者側の仕事ですがそれを事務的にやるものだから、さらに患者さんは突き放されたように受け止めてしまいます。
かなり進行してくると標準的な治療が難しくなって治療法は限られてきます。体力的に化学療法を続けられなくなるとあるところでいきなり「もう治療法はありません」と精神的にも見放されてしまうのが日本のが病院です。 その時点で緩和ケア医やホスピスを見つけるのも難しいですし、結果、多くの人が難民のようにさまよってしまうことになるのです。
治療法がない患者さんに向き合っていくスキルが日本の医療界にはないのです。「目標として、QOLを保ちながら、共存していきましょうと。」とはいうものの、最終的に自分で身の回りのことができなくなったときのことを想定して、病院で治療を継続するのか、在宅などの緩和ケアがいいのか、患者さんが考える機会、時間が少ないように思えます。 緩和ケアの大切さは以前から指摘されているのに、一向に進みません。
がんの進行とともに生じる心のケアも重要です。医師は、患者さんとのコミニケーションが大事なのに不得意な人が多い印象があります。裁量権が比較的大きな職業なので、独占的になりやすいです。受診先を選択するときは、こうしたことを念頭に置き、自分に合った医師を見つけてください。
自分に合う治療法にめぐり合えるのか患者さんは考えてしまいます。結果、自由診療(代替療法)のクリニックに行く要因にもなっています。
標準治療以上に自由診療(代替療法)の治療成績がよいということではありません
代替療法の一つである自由診療は一部を除き、科学的根拠が不明確で、標準治療に比べてはるかに信頼性に劣ります。高額な医療費にもなります。 価格が高いから効果が期待できる訳ではありません。
最近の治療法
最近の治療では、根治の可能性が少ない場合でも薬を変えながら、できるだけ長期間にわたってがんの病変をコントロールして、延命することが目標になっています。作用機序の異なる薬がいろいろあるので、がんの種類、性質、体質、体力を鑑みて、薬の選択や組み合わせを決めたりして治療を進めます。放射線治療も正常細胞にダメージを与えますがそれ以上にがん細胞にダメージを与えます。
上手く長期にわたって副作用がコントロールできれば、通院などで良い体調を保ったままがんになる以前の生活を続けることができるだけでなく、がんで亡くなるのではなく寿命を全うすることもできるからです。
がん組織では、多様ながん細胞がありその中のがん細胞が必ず変異して薬剤耐性を獲得します。がんの分子標的薬は,高い確率で奏効するもののがん細胞内の分子に遺伝子変異が起こり耐性化することが知られています。また免疫チェックポイント阻害薬(PD-1・PD-L1阻害薬)の治療耐性が生じることが明らかになっています。
どの治療法も全ての患者さんに等しく効果があるわけではないことを理解し薬物療法では、病勢の増悪や重い副作用がない限り、現状の治療を継続するのが基本になっています。
頼れるがん治療アドバイザーを目指します
がん治療は専門的な知識や判断が必要であるため、画像検査(CT・MRIなど)病理検査(採取された病変組織の病理学的診断)など踏まえた上で院内カンファレンス(病状検討会)を経て、最終的に主治医からがんの告知を受けます。その後、治療法について十分な説明を受けます。それに対して患者さんは内容をよく理解して疑問があれば解消し、納得した上で医療行為に同意します。しかし、がんの告知を受けた患者さんは精神的にもかなり深刻な状態です 冷静な判断力を失っている場合も多いと思います。丁寧な説明を受けても、それを理解するまでには時間がかかります。
患者さん自身が治療に関して理解を深め、納得した上で選択した治療を進めることができるよういつでもサポートできるアドバイザーになりたいと思っております。悔いの無い治療を心より願っております。
がんの治療は、医師と患者さんとご家族の方の密接な連携が何より大切です。インフォームド・コンセント((納得と治療の選択)の普及の一助となれば大変意義深いことと考えております。
がん治療の現状 手術(外科療法)
がん治療の現状 薬物療法(抗がん剤)
がん治療の現状 放射線療法
がん治療の現状 がん治療の難しい理由
がん治療サポート内容 最善のがん治療を受けるために
「がん治療相談」がん治療アドバイザーによるサポート
オピニオン(がん治癒への道)
がん標準治療を選択するとき
「がん標準治療」生存率
がん先進医療(精密医療)
がん免疫療法
がん発生メカニズム
がん再発・転移
がん幹細胞
がん悪液質(あくえきしつ)
がん遺伝子治療
標準治療以上に自由診療の治療成績がよいということではありません
新型コロナウイルの基本知識